ゴマの健康機能成分配糖体の生合成:最後の"missing piece"の同定
2019/12/05
【概要】
工学研究科バイオ工学専攻応用生命化学講座の研究グループ(和氣駿之 助教ら)は,サントリーグローバルイノベーションセンター,サントリー生命科学財団生物有機科学研究所,南九州大学等との共同研究によって,ゴマの健康機能成分であるセサミノール注1)の配糖体注2)の生合成に関わる糖転移酵素遺伝子を同定し,多酵素複合体(メタボロン)注3)形成を介した同配糖体の生合成の仕組みを提案しました.生合成経路の最後の"missing piece"となっていた酵素遺伝子が同定されたことにより,ゴマ健康機能成分であるセサミノールの含量や種子中での貯蔵形態を制御するバイオテクノロジーの分子基盤が整ったといえます.この共同研究の成果は,12月2日に植物科学専門誌ザ・プラントジャーナルに掲載されました.
【詳細な説明】
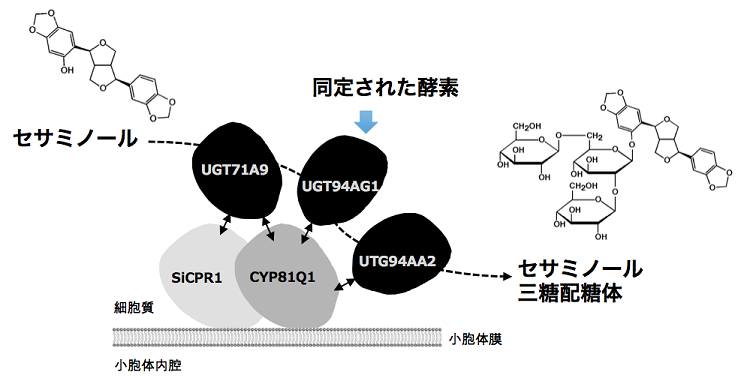
セサミノールはヒトの健康に好ましい数々の効果(抗酸化活性,動脈硬化予防,アルツハイマー病予防等)が期待されているリグナン化合物注1)で,ゴマ種子中では3分子のグルコースが分岐状に結合した三糖配糖体として存在します.その貯蔵場所は液胞と推定されます.脂溶性のセサミノールを液胞に貯蔵するためには,これを水溶性のかたちに変換する必要がありますが,これはセサミノールに糖を付加すること(配糖体化)によって可能となります.すなわち,セサミノールに3個のグルコースを結合することにより貯蔵が可能となっていると考えられます.またセサミノールはそれ自体で上述の生理活性を示しますが,ゴマはこれを配糖体化することによって生理不活性なかたちとして貯えていると考えられます.これまで,この配糖体化の機構の解明が不十分なままでしたが,今回の研究でその全貌が明らかになりました。研究チームは,トランスクリプトーム解析注4)と生化学的手法の組み合わせによって同酵素(UGT94AG1)を新たに同定しました.また,生合成酵素群の間でのタンパク質間相互作用を網羅的に解析し,UGT94AG1をはじめとする糖転移酵素群が,シトクロムP450であるセサミン合成酵素(CYP81Q1)を核にして多酵素複合体を形成することを明らかにしました.さらに3分子のグルコースがセサミノールに結合する際のおもな順序も明らかになりました.今回明らかにされた配糖体化の仕組みを制御することによって,活性型のセサミノールを得ることが可能となると予想され,セサミノール生産への活用が期待されます.
【用語解説】
注1)セサミノールとリグナン
桂皮酸誘導体から導かれる植物特化代謝産物の一群で,C6-C3型の構造が二つ組み合わさった構造をもつものをリグナンという.リグナンは,ゴマなどいくつかの種子作物に豊富に含まれ,セサミンとセサミノールはゴマ特有のリグナンである.
注2)配糖体
糖でない部分に糖が結合したものを配糖体という.
注3)多酵素複合体(メタボロン)
生命現象は,生体内でおびただしい数の化学反応が起こることによって成り立っている.これらの化学反応はほとんどの場合,ある反応の生成物が次の反応の基質になり,その反応生成物がその次の反応の基質になるというように,連続した反応経路を形成している.こうした生体内の反応経路のことを代謝または代謝経路と呼ぶ。代謝経路を構成する反応の一つ一つはそれぞれ,反応加速作用をもつ「酵素」というタンパク質のはたらきによって円滑に進行し,反応が異なれば担当する酵素も異なる.40年ほど前から,代謝経路を構成する酵素群は細胞内ではお互いにゆるく結合しながら複合体を形成しているのではないかと推定されてきた.この酵素複合体のことをメタボロンという.メタボロンを形成することにより,例えば不安定な代謝中間体を速やかに次の酵素に受け渡せたり,有毒な代謝中間体を細胞内に拡散させることなく即座に次の酵素反応に提供することができたりするなど,代謝を進める上で様々な利点があると考えられている.
注4)トランスクリプトーム解析
細胞や組織内におけるすべての遺伝子転写産物(mRNA)の配列解析
【論文情報】
The Plant Journal https://doi.org/10.1111/tpj.14586