iPS細胞による心筋細胞作製を効率化する培養法を確立
- 培養細胞を挟み込む硬さが決め手 -
2023/03/17
発表のポイント
概要
近年、細胞周囲の硬さが細胞の性質に影響を及ぼすことが分かってきました。しかしiPS細胞が周囲の硬さに対してどのような応答をするかはよく分かっていませんでした。
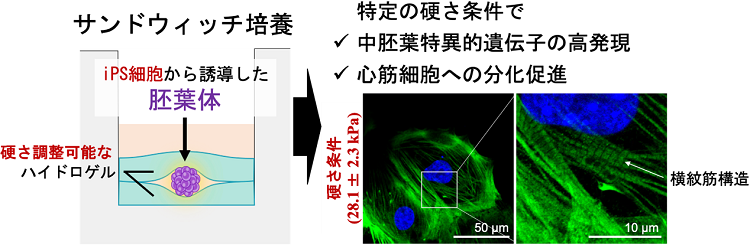
東北大学大学院歯学研究科 分子・再生歯科補綴学分野の大学院生Praphawi Nattasit(パパウィー ナッタシット)さん、新部邦透(にいべ くにみち)講師、江草 宏(えぐさ ひろし)教授および同大大学院工学研究科 山本雅哉(やまもと まさや)教授らの研究グループは、iPS細胞が形成した細胞の塊を、硬さの調節が可能なハイドロゲルで挟みこむ“サンドウィッチ培養法”を確立しました。本培養法を用い、ゲルの硬さを心臓の硬さに近似させると、iPS細胞が中胚葉注3の細胞に分化しやすくなり、拍動する心筋細胞が効率的に得られました。
本研究で確立した培養法は、従来のiPS細胞を用いた心筋細胞作製の効率化に役立つ可能性があります。また、硬さ環境に着目した本培養法は、iPS細胞から様々な組織や器官(培養臓器)を作製するために適した硬さ環境や、その分子機構を明らかにするツールとして活用されることが期待されます。
本研究成果は、2023年3月5日に、高分子科学の専門誌Macromolecular Bioscienceに掲載されました。
研究の背景
人工多能性幹細胞(iPS細胞)は、無限の増殖能と様々な細胞に分化する能力を有し、患者の細胞から作製することができることから、再生医療への応用や、疾患モデルとして薬剤スクリーニングなどへの活用が期待されています。
心筋梗塞や心筋炎などで心臓の心筋細胞が壊死すると、再生能力の乏しい心筋細胞による修復や機能の回復は困難であるため、再生医療が有効な治療法となります。iPS細胞を心筋細胞に分化誘導する方法はいくつか報告されていますが、培養に時間がかかることや、完全に分化していない細胞が残存すると移植先で腫瘍を形成する危険性があることから、より効率的な分化誘導法の開発が求められています。
一方、細胞を取り巻く機械的な刺激や硬さの環境が、幹細胞の遊走や分化の方向性に影響を及ぼすことがわかってきました。しかしながらiPS細胞が硬さ環境に対してどのように応答して分化を調節するのかはよく分かっていません。
今回の取り組み
東北大学大学院歯学研究科 分子・再生歯科補綴学分野のPraphawi Nattasit(パパウィー ナッタシット)さん、新部邦透(にいべ くにみち)講師、江草 宏(えぐさ ひろし)教授および同大大学院工学研究科 山本雅哉(やまもと まさや)教授らの研究グループは、iPS細胞が形成する細胞の塊(胚葉体)を、硬さの調節が可能なポリアクリルアミドハイドロゲルで三次元的に挟みこむことで、“サンドウィッチ培養法”を確立しました。
この培養法をマウスiPS細胞の胚葉体に用いると、ゲルの硬さに応じてYes-associated protein(YAP)注4シグナル伝達経路が活性化され、アクチン細胞骨格の再編成を促すことがわかりました。またゲルの硬さを心臓の硬さに近似させると、iPS細胞は中胚葉の細胞に分化しやすくなり、発生学的に心臓の筋肉が由来する側板中胚葉の関連遺伝子が発現することを突き止めました。さらにこの中胚葉細胞を心筋細胞に誘導したところ、拍動する細胞が多く出現し、構造的にもより成熟した心筋細胞が得られることが明らかになりました。
今後の展開
本研究で確立したサンドウィッチ培養法に特定の硬さ条件を用いることで、従来のiPS細胞を用いた心筋細胞の作製がより効率的に行える可能性があります。また硬さ環境に着目した本培養法は、iPS細胞から様々な組織や器官(培養臓器)を作製するために適した硬さ環境や、その分子機構を明らかにするツールとして活用されることが期待されます。
謝辞
本研究は、JSPS科研費 挑戦的研究・萌芽(JP18K19630)、基盤研究C(JP19K10220)、国際共同研究加速基金(JP17KK0182)、基盤研究B(JP21H03814)、学術変革領域A(JP21H05769)の一環で行われました。
用語説明
(注1)iPS細胞
特定の因子を細胞に導入することで人為的に作られた人工多能性幹細胞。あらゆる細胞から作り出すことが可能であり、倫理的な課題が残されていた胎性幹細胞(ES細胞)に代わる再生医療の細胞源として着目されており、高い増殖能と分化能を有する。再生医療の他、遺伝子疾患等の疾患特異的な細胞モデルを確立することで、薬剤スクリーニングなど医療分野への幅広い応用が期待されている。
(注2)分化
幹細胞が何かしらの役割を担う別の細胞に段階を経ながら分裂・増殖して変化すること。最終的な役割の決まっていないiPS細胞は、「未分化」な状態と呼ぶ。筋肉の細胞や皮膚の細胞など、組織や器官を構成し役割の決まった細胞は分化が終了しており、それぞれの場所で機能を果たす。
(注3)中胚葉
発生が進む段階で、主に骨・軟骨・脂肪・骨格筋などに分化する体節中胚葉、心臓・血管・内臓筋などに分化する側板中胚葉など体を構成する重要な胚葉。表皮や神経系に分化する外胚葉、消化管に分化する内胚葉と合わせて、動物の発生の初期段階で区別される三胚葉のうちの1つ。
(注4)Yes-associated protein(YAP)
転写因子として機能するタンパク質。細胞増殖やアポトーシスに関与するだけでなく、発生過程における器官の大きさの制御や胚の発生などに関与することが知られている。
論文情報
著者: Praphawi Nattasit, Kunimichi Niibe*, Masahiro Yamada, Yumi Ohori-Morita, Phoonsuk Limraksasin, Watcharaphol Tiskratok, Masaya Yamamoto and Hiroshi Egusa*
*責任著者: 東北大学大学院歯学研究科 講師 新部 邦透, 教授 江草 宏
掲載誌: Macromolecular Bioscience
DOI: 10.1002/mabi.202300021