DNAナノポアセンサでオーダーメイドに分子を検出!
- 創薬や診断に役立つバイオセンサの創出に向けて -
2025/05/08
本研究成果のポイント
研究の概要
長岡技術科学大学 技学研究院 機械系の庄司 観准教授、大学院工学研究科 先端工学専攻 材料工学分野の赤井 大夢(博士後期課程3年、函館工業高等専門学校出身)は、東北大学 流体科学研究所の馬渕 拓哉准教授、大学院工学研究科の平野 太一(博士後期課程1年)と共同で、分子を選択的に検出できる「DNAナノポアセンサ」を開発しました。
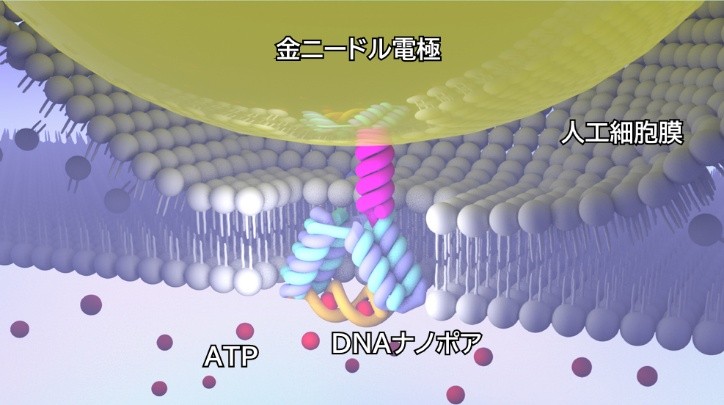
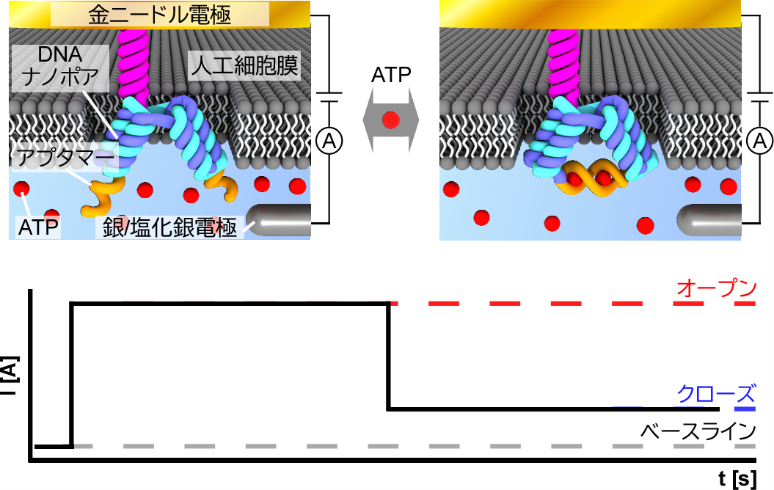
本センサに応用したDNAナノポアは、人工細胞膜中でイオンの通り道として働く膜貫通ドメインと、標的分子であるアデノシン三リン酸(ATP)に選択的に結合する機能を持つ核酸分子であるATP結合アプタマー(注4)で構成されています。本研究グループは、ATPとアプタマーの結合・解離による膜貫通ドメインの可逆的な開閉動作を、ナノポアを通過するイオン電流の変化として計測することで、ATPの選択的検出に成功しました(図1)。本技術は、アプタマーの塩基配列を変更することで様々な生体分子に応用できる可能性を有しており、創薬や疾患診断などの分野へのナノポア計測技術の応用展開を促進することが期待されます。
研究の背景
ナノポアセンサは、薄膜上に構築されたナノメートルスケールの細孔と標的分子の相互作用によるイオン電流の変化から標的分子を検出できる、非標識かつ高時空間分解能を持つ一分子計測技術です。原理上、ナノポアを通過する様々な分子が検出されるため、標的分子のみを検出するには、標的分子の物理的または化学的特性に合わせたオーダーメイドのナノポアが必要となります。そこで近年、サイズ・形状・機能性を自在に制御できる「DNAナノポア」のナノポアセンサへの応用が期待されています。これまでに分子に応答した開閉動作を誘発可能なDNAナノポアは報告されていましたが、センサ応用に必要不可欠である分子選択性や濃度依存性に関するナノポアの特性評価は実施されておらず、ナノポアセンサとしての応用可能性は不明でした。この問題は、DNAナノポアの人工細胞膜(注5)への挿入効率が低いため、イオン電流計測によるナノポアの特性評価実験の効率も低くなってしまうことが原因でした。
研究の成果
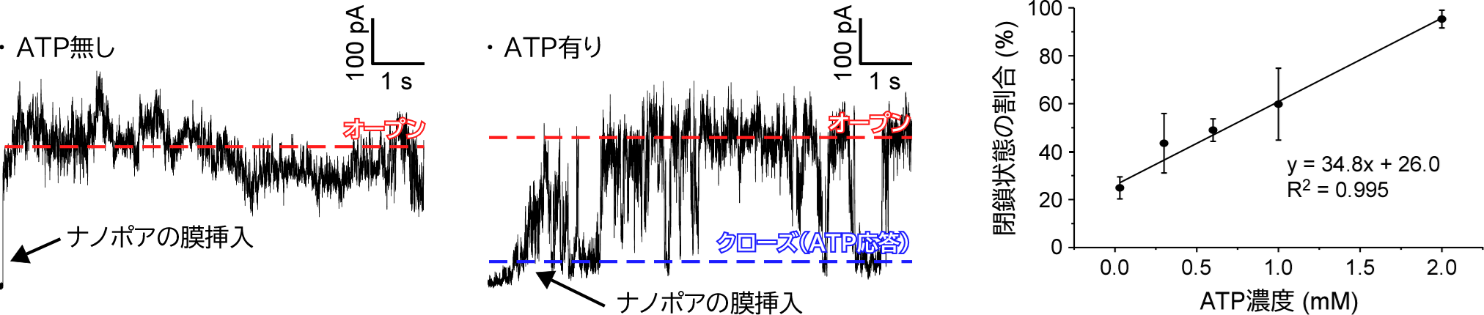
本研究では、構造DNAナノテクノロジーを用いて、ATPに選択的に応答してダイナミックに開閉するDNAナノポアセンサを開発しました。そして、本研究グループが開発した、金ニードル電極の先端に固定化したDNAナノポアを物理的に人工細胞膜に挿入する「DNAナノポアプローブ技術」(参考文献①)を用いて、DNAナノポアを人工細胞膜に高効率に挿入しイオン電流を計測することで、ATPに応答したDNAナノポアの開閉動作の観察に成功しました(図2)。また、従来の研究では、DNAナノポアの開閉動作に分子濃度依存性があるかは不明でしたが、本研究により、ATP濃度に依存して、閉鎖状態(アプタマーとATPが結合している状態)の割合が変化することが分かりました(図3)。さらに、原子レベルの構造変化を観察できる分子動力学シミュレーション(注6)を用いることで、DNAナノポアのATP応答的な開閉メカニズムの詳細を明らかにしました。
今後の展開
ナノポアセンシングは、非標識かつ高時空間分解能を持つ一分子計測技術であり、小分子、核酸やタンパク質などの生体分子だけでなく、細胞やプラスチックなど幅広い物質の検出へと応用範囲が広がっています。本研究で開発したDNAナノポアセンサは、アプタマーの修飾により、標的分子のみを検出できる高い分子選択性を獲得しました。アプタマーは、塩基配列を変更することで、生体分子・細胞・プラスチックなどの様々な物質に対して選択的に結合することができるため、DNAナノポアセンサはあらゆる標的物質の検出に応用できる汎用的ナノポアセンサとして利用されることが期待されます。今後は、本研究グループで開発している走査型プローブ顕微鏡技術(参考文献②)と組み合わせて、ナノポアの位置を精密に制御することで、細胞内外の様々な物質の局所的かつ選択的な計測を実現し、創薬や疾患診断の分野に貢献できる汎用的ナノポアセンシング技術の構築を目指します。
論文情報
著者: Hiromu Akai, Taichi Hirano, Takuya Mabuchi and Kan Shoji
掲載誌: Small(電子版2025年5月2日付)
DOI: 10.1002/smll.202409293
謝辞
本研究は、科学研究費助成事業 基盤研究B(課題番号:23H01822)、学術変革領域研究(A)(課題番号:23H04396)、文部科学省 卓越研究員事業、科学技術振興機構(JST) 創発的研究支援事業(課題番号:JPMJFR2028、JPMJFR212H)および、ムーンショット型研究開発事業(課題番号:JPMJMS2217)の支援により実施されました。
用語説明
(注1)DNAナノポア
DNAで構築されたナノメートルスケールの細孔。人工細胞膜に挿入されるとイオンの通り道として働く。
(注2)ナノポアセンサ
ナノポアと標的分子の相互作用によるイオン電流の変化から、標的分子を検出する技術。
(注3)アデノシン三リン酸(ATP)
生体内の化学反応を引き起こすエネルギー源として用いられる小分子。
(注4)アプタマー
特定の分子と結合して立体構造を構築する核酸分子。塩基配列次第で様々な分子を標的とすることができる。
(注5)人工細胞膜
リン脂質の自己組織化により構築される薄膜。
(注6)分子動力学シミュレーション
原子レベルで設計した分子の動きを、物理法則に従ってコンピュータ上で解析する方法。
参考文献
- ①S Ikarashi, H Akai, H Koiwa. et al. “DNA Nanopore-Tethered Gold Needle Electrodes for Channel Current Recording,” ACS Nano, vol. 17, no. 11, pp. 10598-10607, 2023.
- ②R. Yoshihara, S. Nomi, and K. Shoji, “Nanopore Probes Using Hydrogel-Filled Nanopipettes as Sensors for Chemical Imaging,” ACS Appl. Nano Mater., vol. 5, no. 10, pp. 15808–15816, 2022.