NEWS
2007/11/30金属フロンティア工学専攻の前川准教授、先端学術融合工学研究機構の高村准教授らの共同研究グループは世界初の固体状の水素化物がリチウム超イオン伝導を示すことを発見しました。
【研究の背景】
リチウムボロハイドライド(LiBH4)は、リチウム(Li)、ホウ素(B)、水素(H)、から構成される水より軽い固体状の水素化物であり、化学合成の分野では還元剤などとして利用されてきました。最近では、LiBH4 の結晶に含まれる高密度の水素に注目した水素貯蔵材料としての研究開発も進行しており、エネルギー関連の多様な機能設計やそれに必要な物性解析が重要な研究テーマとなっていました。
【研究成果の概要】
国立大学法人東北大学(総長:井上明久)金属材料研究所(所長:中嶋一雄)の松尾元彰RA(東北大学グローバルCOE リサーチアシスタント、環境科学研究科博士後期課程)、中森裕子助教、折茂慎一准教授、および同大学院工学研究科(研究科長:内田龍男)の前川英己准教授、先端学術融合工学研究機構の高村仁准教授の共同研究チームでは、LiBH4 の電気伝導(=結晶内部でのイオンや電子の長距離移動)および核磁気共鳴(=主にリチウムイオンの短距離移動)などの測定から、388K(115℃)付近での結晶構造の変化に伴ってリチウムイオンが1000 倍も移動しやすくなる現象を世界で初めて観測しました。
この現象は、次のように理解することができます:
- LiBH4の結晶は、リチウムイオン(=小さなプラスイオン)とホウ素-水素が結合した錯イオン(=大きなマイナスイオン)から構成されている。
- 通常の結晶では、ホウ素-水素の錯イオンが邪魔になって、リチウムイオンの移動は制限されている。
- 388K(115℃)付近で結晶構造が変化すると、リチウムイオンとホウ素-水素の錯イオンとの位置関係が変わり、リチウムイオンが劇的に移動しやすくなる(=LiBH4 が「リチウム超イオン伝導機能」を示す)。
今回の共同研究の成果は、携帯電話やパソコンなどで広く民生・産業利用されている「リチウムイオン二次電池」の安全性を高めるための新たな固体電解質(=リチウムイオンを高速で移動させることが可能な固体材料)の開発などへの幅広い展開が期待されます。本共同研究の一部は、科学研究費補助金(基盤研究A:18206073)、グローバルCOE プログラム(B03、東北大学、代表 金属材料研究所教授:後藤 孝)からの助成を受けており、詳細は米専門誌「Applied Physics Letters(11 月27 日(現地)、オンライン版)」で公開されました。
【研究成果の詳細】
1) LiBH4に関するエネルギー関連の機能設計や物性解析が重要なテーマ
リチウムボロハイドライドLiBH4 は、比重0.66g/cm2 の軽量な水素化物(550K付近で液化、750〜800K 付近で分解・水素放出)であり、化学合成の分野では還元剤などとして有効利用されてきました。最近では、燃料電池用の高密度水素貯蔵材料として注目されており、元素置換や複合化により水素貯蔵性能の向上(水素放出反応の低温化や高速度化など)が図られています。また、家庭用電子レンジと同じ周波数・出力のマイクロ波(2.45GHz・400W)を吸収して自己発熱することで、急速に水素放出する現象(最速5 分以内)も見出されています。さらに、核融合炉用の新たな中性子遮蔽材料としての研究も、関連する水素化物を用いて進められています。このように、LiBH4 は古くから知られている(また一般に入手できる)水素化物であるにもかかわらず、エネルギー関連の多様な機能設計やそれに必要な物性解析が最近の重要な研究 テーマとなっています。
2) 結晶構造の変化に伴いLiBH4 の電気伝導性が約1000 倍も増大することを発見
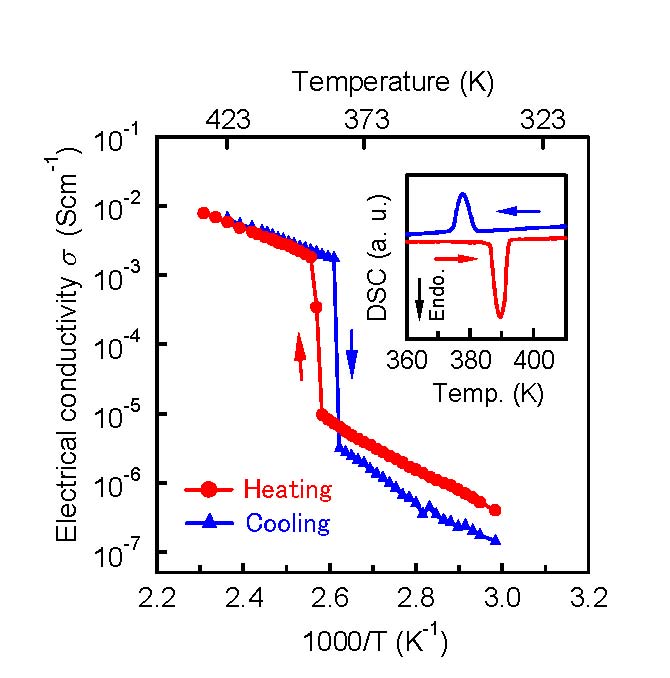
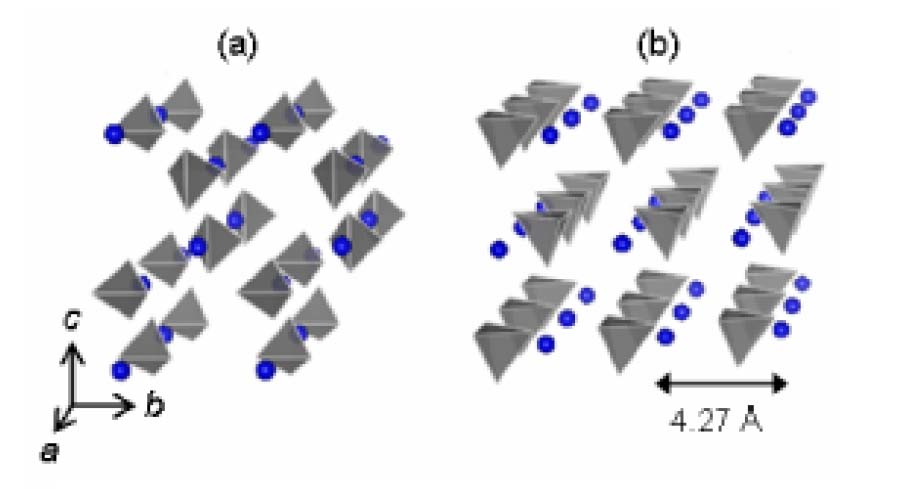
交流インピーダンス法を用いて測定したLiBH4の電気伝導性を図1 に示します。温度上昇(図の右から左)とともに電気伝導率は連続的に大きくなりますが、388 (115℃)前後での結晶構造の変化(図2、(a)室温相→(b)高温相)に伴い、電気伝導性が1000 倍程度も急激に増大して10-3 Scm-1 のオーダーに達することがわかります。(この現象は温度上昇・低下に伴い可逆的に進行します。)電気伝導は「電子伝導」または「イオン伝導」に分類されますが、室温相・高温相ともに絶縁体であることを考えと、LiBH4 の電気伝導は「イオン伝導」によるものと推測されます。さらに、LiBH4 のホウ素(B)と水素(H)は共有結合により安定な錯イオン[BH4]−を形成していることもあわせて考えますと、図1 の388 K(115℃)以上での電気伝導性は「リチウムイオンによるイオン伝導」に起因する可能性が高いといえます。
3) LiBH4 が「リチウム超イオン伝導機能」を示すことを世界で初めて明らかに
上述2)で推測した「リチウムイオンによるイオン伝導」を明確化するために、LiBH4 でのリチウムイオンの短距離移動の様子を核磁気共鳴(7Li NMR)法で解析しました。そして、リチウムイオンのジャンプ距離(高温相におけるLi-Li 間の最近接距離4.27(遵ァ)(1遵ァ(オングストローム)=1 千万分の1ミリメートル)の相関時間を用いて電気伝導性を見積もった結果、図1 の交流インピーダンス法を用いて測定した結果と非常に良い一致を示しました。これにより、高温相における10-3Scm-1のオーダーにも達する高い電気伝導性は「リチウムイオンによるイオン伝導」に起因すること、すなわちLiBH4 が「リチウム超イオン伝導機能」を示すこと、を世界で初めて明らかにすることができました。
4) 研究成果の重要性・発展性
今回の共同研究の成果は、携帯電話やパソコンなどで広く民生・産業利用されている「リチウムイオン二次電池」の安全性を高めるための新たな固体電解質(=リチウムイオンを高速で移動させることが可能な固体材料)の開発などへの幅広い展開が期待されます。従来のリチウムイオン二次電池は、液体(有機系)電解質を用いているために、短絡や過充電などへの対策が不可欠でした。そこで近年、安全性を高めるための固体電解質として有望な新たなリチウムイオン伝導材料の探索が国内外で鋭意進められています。今回、水より軽い固体状の水素化物(リチウムボロハイドライド、LiBH4)での「リチウム超イオン伝導機能」が明らかとなったことで、「固体電解質としての水素化物」の研究開発が活発化するものと予想されます。
共同研究グループでは、現在、リチウムイオン二次電池の構成材料としての特性評価や388K(115℃)以下でも高温相の結晶構造を安定化させる(=室温でリチウム超イオン伝導機能を発現させる)ための材料設計を進めています。
[お問い合わせ先]
東北大学 工学研究科 情報広報室
TEL:022−795−5898 FAX:022−795−5898
E-mail:eng-pr@eng.tohoku.ac.jp
【お問合せ】
東北大学工学研究科・工学部情報広報室
TEL/ FAX:022-795-5898
E-mail:eng-pr@eng.tohoku.ac.jp